로그인
 로그인을 하시면 메디칼타임즈의
로그인을 하시면 메디칼타임즈의다양한 연관서비스를 이용하실 수 있습니다. 가입 시 등록한 정보를 입력해주세요.
 개인정보 보호를 위한 비밀번호 변경안내
주기적인 비밀번호 변경으로 개인정보를 지켜주세요.
개인정보 보호를 위한 비밀번호 변경안내
주기적인 비밀번호 변경으로 개인정보를 지켜주세요.안전한 개인정보 보호를 위해 3개월마다 비밀번호를 변경해주세요. ※ 비밀번호는 마이페이지에서도 변경 가능합니다.
30일간 보이지 않기
- 제약·바이오
- 국내사
생동성 위수탁 급증, 원인은 블록버스터 특허 만료
발행날짜: 2017-03-30 12:00:13
-
가
-
지난해 위수탁품목 비율 67% 돌파…"트윈스타 제네릭 개발 열기"
지난해 생동성시험자료 처리건수가 451건으로 전년도 341건 대비 32% 증가한 것으로 나타났다.
특히 블록버스터 고혈압치료제 트윈스타의 재심사 만료로 다수의 제약사가 제네릭 개발에 뛰어들면서 위수탁품목 비율이 20%나 늘어났다.
30일 식품의약품안전처는 2016년 제네릭의약품 심사보고서를 발간하고 제네릭의약품 심사현황, 주요 보완사항, 심사자료 작성요령 등 최근 의약품 개발 동향을 공유했다.
주요 내용은 ▲2016년 제네릭의약품 심사현황 ▲품질심사, 생물학적동등성시험, 비교용출시험자료 관련 주요 보완사항 ▲심사자료 준비 시 중점 고려사항 ▲심사자료 작성 요령 등이다.
먼저 생물학적동등성 시험 심사 현황을 보면 16년 제네릭의약품 허가, 신고(변경)를 위한 생물학적동등성시험 자료는 총 565품목이 심사대상이었으며 이 중 451품목이 처리됐다.
자료보완 없이 적합 처리된 품목은 317건(70.3%), 자료보완 요구된 품목은 125건(27.7%)을 차지했다.
최종적으로 적합 처리된 품목은 442건(98.0%), 취하된 품목은 9건(2.0%)이었다.
2016년 의약품 허가·신고(변경)를 위한 생물학적동등성시험 자료 처리건수 451건 중 의약품 신규 품목허가 신청은 314(69.4%)건, 허가 후 변경 신청은 97건(21.5%), 사전검토는 40건(9.1%)이었다.
2016년 처리건수 451건 중 위수탁 품목은 235건(52.1%)으로 2015년 115건(33.7%) 대비 큰 폭으로 증가했다.
이는 의약품의 품목허가, 신고 심사규정 개정으로 2016년 3월부터 제네릭의약품도 국제공통기술문서 작성 대상으로 포함돼 시행 시점 이전 민원신청 급증에 따라 증가한 것으로 풀이된다.
재심사 기간 만료에 따라 텔미사르탄/암로디핀베실산염 복합제 90품목(위탁 71품목 포함), 라코사미드 성분 13품목, 리세드론산나트륨/콜레칼시페롤농축물 복합제 26품목(위탁 20품목 포함) 등의 처리건수가 상승한 것으로 분석된다.
한편 위수탁품목 비율도 증가했다.
2016년 최종 처리된 제네릭의약품 품질심사 2,156건 중 사전검토는 184건(8.53%)이고, 품목허가(변경)신청을 위한 심사는 1,972건(91.5%)이었다.
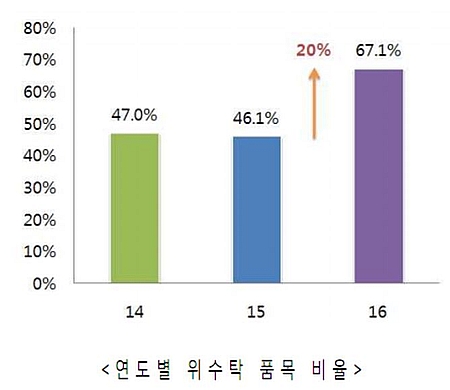
연도별 위수탁품목 비율은 2014년 47.0%, 2015년 46.1%, 2016년 67.1%다.
위수탁품목은 예년에 비해 약 20% 증가한 것으로 나타났으며, 이는 고혈압치료제 블록버스터 제품인 텔미사르탄과 암로디핀베실산염 복합제인 트윈스타가 2016년 8월에 재심사기간이 만료됨에 따라 증가한 것으로 분석된다.
실제로, 동 제품의 제네릭의약품은 2016년 9월 30일 하루 동안 83개 품목이 허가되는 등 현재까지 약 150여 품목이 허가됐다.
특히 블록버스터 고혈압치료제 트윈스타의 재심사 만료로 다수의 제약사가 제네릭 개발에 뛰어들면서 위수탁품목 비율이 20%나 늘어났다.
30일 식품의약품안전처는 2016년 제네릭의약품 심사보고서를 발간하고 제네릭의약품 심사현황, 주요 보완사항, 심사자료 작성요령 등 최근 의약품 개발 동향을 공유했다.
주요 내용은 ▲2016년 제네릭의약품 심사현황 ▲품질심사, 생물학적동등성시험, 비교용출시험자료 관련 주요 보완사항 ▲심사자료 준비 시 중점 고려사항 ▲심사자료 작성 요령 등이다.
자료보완 없이 적합 처리된 품목은 317건(70.3%), 자료보완 요구된 품목은 125건(27.7%)을 차지했다.
최종적으로 적합 처리된 품목은 442건(98.0%), 취하된 품목은 9건(2.0%)이었다.
2016년 의약품 허가·신고(변경)를 위한 생물학적동등성시험 자료 처리건수 451건 중 의약품 신규 품목허가 신청은 314(69.4%)건, 허가 후 변경 신청은 97건(21.5%), 사전검토는 40건(9.1%)이었다.
2016년 처리건수 451건 중 위수탁 품목은 235건(52.1%)으로 2015년 115건(33.7%) 대비 큰 폭으로 증가했다.
이는 의약품의 품목허가, 신고 심사규정 개정으로 2016년 3월부터 제네릭의약품도 국제공통기술문서 작성 대상으로 포함돼 시행 시점 이전 민원신청 급증에 따라 증가한 것으로 풀이된다.
재심사 기간 만료에 따라 텔미사르탄/암로디핀베실산염 복합제 90품목(위탁 71품목 포함), 라코사미드 성분 13품목, 리세드론산나트륨/콜레칼시페롤농축물 복합제 26품목(위탁 20품목 포함) 등의 처리건수가 상승한 것으로 분석된다.
한편 위수탁품목 비율도 증가했다.
2016년 최종 처리된 제네릭의약품 품질심사 2,156건 중 사전검토는 184건(8.53%)이고, 품목허가(변경)신청을 위한 심사는 1,972건(91.5%)이었다.
연도별 위수탁품목 비율은 2014년 47.0%, 2015년 46.1%, 2016년 67.1%다.
위수탁품목은 예년에 비해 약 20% 증가한 것으로 나타났으며, 이는 고혈압치료제 블록버스터 제품인 텔미사르탄과 암로디핀베실산염 복합제인 트윈스타가 2016년 8월에 재심사기간이 만료됨에 따라 증가한 것으로 분석된다.
실제로, 동 제품의 제네릭의약품은 2016년 9월 30일 하루 동안 83개 품목이 허가되는 등 현재까지 약 150여 품목이 허가됐다.

관련기사
- 트윈스타 제네릭 185개 각축…눈도장 찍는 비법은? 2017-02-01 05:00:55
- 이레사정·트윈스타 제네릭 대전…약가 경쟁 예고 2016-11-26 05:00:33
- 트윈스타 제네릭 줄줄이 승인…12월 대전 본격화 2016-10-01 05:00:10
- "돈 되는 제네릭에 집중" 리나글립틴 개발 최다 2017-02-21 11:44:25
제약·바이오 기사
- 고혈압 복합제 선택 고민이세요? 5분만 들어주세요 2017-03-30 12:00:57
- '타프' 앞세운 길리어드…포트폴리오 새판짜기 2017-03-30 05:00:33
- 자누비아 패밀리 제형 추가…신장애 환자 겨냥 2017-03-29 11:58:43
- 면역항암제 경쟁 화이자 합류…후발주자 승부수 2017-03-29 11:55:04
- "듀비에 넘보지 마" 종근당, 조성물 특허 취득 2017-03-29 11:13:57
제약·바이오 기사
많이 읽은 뉴스
이메일 무단수집 거부
메디칼타임즈 홈페이지에 게시된 이메일 주소가 전자우편 수집 프로그램이나
그 밖의 기술적 방법을 이용하여 무단으로 수집되는 것을 거부하며,
이를 위반할 시에는 정보통신망법에 의해 형사 처벌될 수 있습니다.
그 밖의 기술적 방법을 이용하여 무단으로 수집되는 것을 거부하며,
이를 위반할 시에는 정보통신망법에 의해 형사 처벌될 수 있습니다.









- 최신순
- 추천순
댓글운영규칙ex) medi****** 아이디 앞 네자리 표기 이외 * 처리
댓글 삭제기준 다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입이 제한될 수 있습니다.
1. 저작권・인격권 등 타인의 권리를 침해하는 경우
2. 상용프로그램의 등록과 게재, 배포를 안내하는 게시물
3. 타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
4. 욕설 및 비방, 음란성 댓글